Unterschied zwischen Methan und Ethan | Methan vs Ethan
Unterschied zwischen Methan und Ethan, Methan und Ethan, Methan und Ethan, Methan und Ethan, Methan und Ethan vs Ethan
Methan und Ethan sind die kleinsten Vertreter der Alkan-Familie. Die Molekularformeln dieser beiden organischen Verbindungen sind CH 999 4 999 bzw. C 999 2 999 H 999 6 999. Der Schlüsselunterschied zwischen Methan und Ethan ist ihre chemische Struktur ; kann ein Ethan-Molekül als zwei Methylgruppen angesehen werden, die als Dimer von Methylgruppen verbunden sind. Die anderen chemischen und physikalischen Unterschiede ergeben sich hauptsächlich aufgrund dieser strukturellen Unterschiede. Was ist Methan? Methan ist das kleinste Mitglied der Alkanfamilie mit der chemischen Formel CH 4 (vier Wasserstoffatome sind an ein Kohlenstoffatom gebunden). Es gilt als Hauptbestandteil von Erdgas. Methan ist ein farbloses, geruchloses und geschmackloses Gas. auch bekannt als Carban, Sumpfgas, Erdgas, Kohlentetrahydrid,
undWasserstoffkarbid
. Es kann leicht gezündet werden, und sein Dampf ist leichter als die Luft.
H 6 bzw. 30,07 g · mol
-1
. Es wird aus Erdgas als Nebenprodukt aus der Erdölraffination isoliert. Ethan ist bei der Ethylenherstellung sehr wichtig.

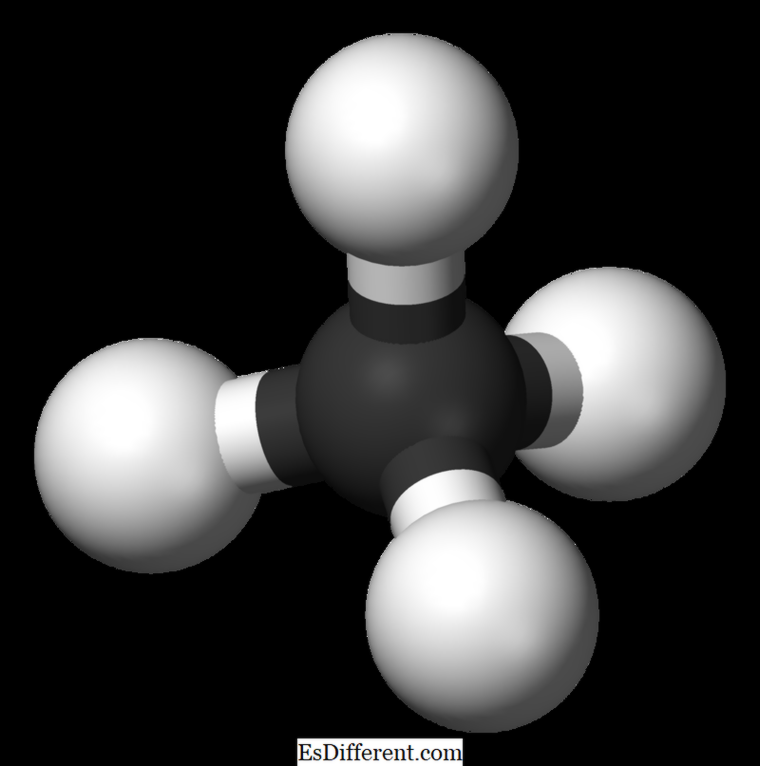
von Methan ist
CH
4,
eines tetraedrischen Moleküls mit vier äquivalenten CH-Bindungen (Sigma-Bindungen). Der Bindungswinkel zwischen den H-C-H-Atomen beträgt 109. 5 0 und alle CH-Bindungen sind gleichwertig und gleich 108. 70 Uhr. Ethan: Die Molekularformel von Ethan ist C 2

H 6, und ist ein gesättigter Kohlenwasserstoff, enthalten mehrere Bindungen. Chemische Eigenschaften: Methan: Stabilität: Methan ist chemisch sehr stabil und reagiert nicht mit KMnO < 2 O 7

, H
2
SO 4 oder HNO 3 unter normalen Bedingungen. Verbrennung: In Gegenwart von überschüssiger Luft oder Sauerstoff verbrennt Methan mit einer hellblauen, nicht leuchtenden Flamme, die Kohlendioxid und Wasser produziert.Es ist eine stark exotherme Reaktion; Daher wird es als hervorragender Kraftstoff verwendet. In Gegenwart von unzureichender Luft oder Sauerstoff verbrennt es teilweise zu Kohlenmonoxid (CO) -Gas. Substitutionsreaktionen: Methan zeigt Substitutionsreaktionen mit Halogenen. Bei diesen Reaktionen werden ein oder mehrere Wasserstoffatome durch eine gleiche Anzahl von Halogenatomen ersetzt und es wird als "Halogenierung" bezeichnet. "Es reagiert mit Chlor (Cl) und Brom (Br) in Gegenwart von Sonnenlicht. Reaktion mit Dampf: Wenn ein Gemisch aus Methan und Wasserdampf durch ein erhitztes (1000 K) Nickel auf Aluminiumoxidoberfläche geleitet wird, kann es Wasserstoff erzeugen. Pyrolyse: Wenn Methan auf etwa 1300 K erhitzt wird, zerfällt es in Ruß und Wasserstoff. Ethan: Reaktionen: Ethangas reagiert mit Bromdampf in Gegenwart von Licht zu Bromethan (CH
> 3 CH
2 Br) und Bromwasserstoff (HBr). Es ist eine Substitutionsreaktion; ein Wasserstoffatom in Ethan ist durch ein Bromatom substituiert.
CH 3
CH 3
+ Br
2 CH 3 CH 2 Br + HBr Verbrennung: Die vollständige Verbrennung von Ethan erzeugt 1559. 7 kJ / mol (51. 9 kJ / g) Wärme, Kohlendioxid und Wasser. 2 C 2 H
6 + 7 0 2 → 4 CO 2 + 6 H 2 O + 3120 kJ
Es kann auch ohne Sauerstoffüberschuss auftreten und eine Mischung aus amorphem Kohlenstoff und Kohlenmonoxid erzeugen. 2 C
2 H 6 + 3 O 2 → 4 C + 6 H 2 O + Energie 2 C 2 H 6 + 59999 0 999 2 4 CO + 6 999 H 2 O + Energie 2 C 999 2 999 H 999 69999 + 4 999 0 999 2 999 2 C + 2 CO + H
2
O + Energie usw. Definitionen: Substitutionsreaktionen: Die Substitutionsreaktion ist eine chemische Reaktion, bei der eine funktionelle Gruppe in eine chemische Verbindung ersetzte es durch eine andere funktionelle Gruppe. Verwendet: Methan: Methan wird in vielen industriellen chemischen Prozessen (als Treibstoff, Erdgas, verflüssigtes Erdgas) eingesetzt und als Kühlfluid transportiert. Ethan: Ethan wird als Treibstoff für Motoren und als Kältemittel für ein System mit extrem niedrigen Temperaturen verwendet. Es wird in Stahlflaschen als verflüssigtes Gas unter eigenem Dampfdruck ausgeliefert. Referenzen: "Ethan".
Wikipedia . N. p., 2016. Web. 7. Juni 2016. Khanna, Bhishm. "Was sind die chemischen Eigenschaften von Methan? ". Preservearticles. com . N. p., 2016. Web. 7. Juni 2016. "Methan | CH4 - Pubchem ". Pubchem. ncbi. nlm. nih. gov . N. p., 2016. Web. 7. Juni 2016. "Methan". Wikipedia . N. p., 2016. Web. 7. Juni 2016. Bild Courtesy: "Ball-und-Stick-Modell des Methan-Moleküls" von (Public Domain) via Commons Wikimedia "Ball und Stick Modell von Ethan Molekül" y Ben Mills - Eigenes Werk (Public Domain) via Commons Wikimedia "Methan" von Jynto - Eigene Arbeit, basierend auf File: Methan-CRC-MW-Dimensionen-2D.(Public Domain) über Commons Wikimedia


