EDTA gegen EGTA
EDTA und EGTA sind beide Chelatbildner. Beide sind Polyaminocarbonsäuren und haben mehr oder weniger die gleichen Eigenschaften.
EDTA
EDTA ist der verkürzte Name für Ethylendiamintetraessigsäure. Es ist auch bekannt als (Ethylendinitrilo) tetraessigsäure. Es folgt die Struktur von EDTA.
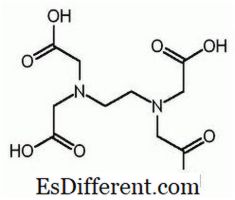
Das EDTA-Molekül hat sechs Stellen, an denen ein Metallion gebunden werden kann. Es gibt zwei Aminogruppen und vier Carboxylgruppen. Die zwei Stickstoffatome der Aminogruppen haben jeweils ein nicht-substituiertes Elektronenpaar. EDTA ist ein hexadentatischer Ligand. Außerdem ist es ein Chelatbildner aufgrund der Fähigkeit, Metallionen zu sequestrieren. EDTA bildet Chelate mit allen Kationen außer Alkalimetallen und diese Chelate sind ausreichend stabil. Die Stabilität ergibt sich aus den verschiedenen Komplexierungsstellen innerhalb des Moleküls, die zu einer käfigartigen Struktur führen, die das Metallion umgibt. Dies isoliert das Metallion von den Lösungsmittelmolekülen und verhindert so die Solvatation. Die Carboxylgruppe von EDTA kann dissonierende Protonen dissoziieren; EDTA hat daher saure Eigenschaften. Die verschiedenen EDTA-Spezies werden mit H 4 Y, H 3 Y - abgekürzt H 999 2 999 Y 999 2-, HY3 - und Y 4- . Bei sehr niedrigem pH-Wert (saures Medium) ist die protonierte Form von EDTA (H 4 Y) vorherrschend. Im Gegensatz dazu überwiegt bei hohem pH (basisches Medium) die vollständig deprotonierte Form (Y 4-999). Und da sich der pH-Wert von einem niedrigen pH-Wert zu einem hohen pH-Wert ändert, dominieren andere EDTA-Formen in bestimmten pH-Werten. EDTA ist als vollständig protonierte Form oder als Salzform erhältlich. Dinatrium-EDTA und Calcium-Dinatrium-EDTA sind die gebräuchlichsten verfügbaren Salzformen. Die freie Säure H 999 4 999 Y und das Dihydrat des Natriumsalzes Na 999 2 999 H 999 2 999 Y. 2H 2 O sind in Reagensqualität im Handel erhältlich.
EDTA wirkt beim Auflösen in Wasser wie eine Aminosäure. Es existiert als Doppelzwitterion. Bei dieser Gelegenheit ist die Nettoladung Null, und es gibt vier dissoziierbare Protonen (zwei Protonen sind mit den Carboxylgruppen assoziiert und zwei mit Aminogruppen verbunden). EDTA wird häufig als komplexometrisches Titriermittel verwendet. EDTA-Lösungen sind als Titrationsmittel wichtig, weil sie unabhängig von der Ladung des Kations mit Metallionen im Verhältnis 1: 1 kombiniert werden. EDTA wird auch als Konservierungsmittel für biologische Proben verwendet. Die geringen Mengen an Metallionen, die in biologischen Proben vorhanden sind, und Nahrungsmittel können die Luftoxidation von Verbindungen, die in den Proben vorhanden sind, katalysieren. EDTA komplexiert diese Metallionen und verhindert so, dass sie die Luftoxidation katalysieren. Deshalb kann als Konservierungsmittel verwendet werden.
EGTA EGTA ist die Abkürzung für Ethylenglykoltetraessigsäure. Es ist ein Chelatbildner und sehr ähnlich wie EDTA.EGTA hat eine höhere Affinität zu Calciumionen als Magnesiumionen. EGTA hat die folgende Struktur. Ähnlich wie EDTA besitzt EGTA auch vier Carboxylgruppen, die nach Dissoziation vier Protonen produzieren können. Es gibt zwei Aminogruppen, und die zwei Stickstoffatome der Aminogruppen haben jeweils ein nicht-geteiltes Elektronenpaar. EGTA kann als Puffer verwendet werden, um dem pH-Wert einer lebenden Zelle zu ähneln. Diese Eigenschaft von EGTA erlaubt seine Verwendung in der Tandem-Affinitätsreinigung, bei der es sich um eine Proteinreinigungstechnik handelt. Was ist der Unterschied zwischen EDTA und EGTA ? • EDTA ist Ethylendiamintetraessigsäure und EGTA ist Ethylenglykoltetraessigsäure. • EGTA hat ein höheres Molekulargewicht als EDTA. • Außer den vier Carboxylgruppen, zwei Aminogruppen, hat EGTA noch zwei weitere Sauerstoffatome mit nicht-geteilten Elektronen.
• EGTA hat eine höhere Affinität zu Calciumionen im Vergleich zu EDTA. Und EDTA hat eine höhere Affinität zu Magnesium-Ionen im Vergleich zu EGTA.
• EGTA hat einen höheren Siedepunkt als EDTA.





