Unterschied zwischen Säure-Base-Titration und Redox-Titration | Säure-Base-Titration vs. Redox-Titration
Schlüsseldifferenz - Säure-Base-Titration vs. Redox-Titration < Titrationen werden zur Bestimmung der Konzentration einer unbekannten Lösung (Analyt) verwendet. Die am häufigsten verwendeten zwei titrimetrischen Methoden sind Säure-Base-Titrationen und Redox-Titrationen. Der
Schlüsselunterschied zwischen Säure-Basen-Titrationen und Redoxtitrationen ist die Art der Reaktion zwischen Titriermittel und Analyt bei der Titration. Bei Säure-Base-Titrationen findet eine Neutralisationsreaktion statt und bei Redoxtitrationen findet eine Redoxreaktion statt (eine Oxidationsreaktion und eine Reduktionsreaktion). Die Verwendung von Indikatoren ist die am häufigsten verwendete Methode zur Bestimmung des Endpunkts der Reaktion.
Was ist eine Säure-Base-Titration?Bei Säure-Base-Titrationen wird als Titriermittel eine Säure (saure Titrationen) oder eine Base (Basistitrationen) verwendet. Beispiele für Säuren, die bei sauren Titrationen verwendet werden, sind H
2 SO 4 , HCl oder HNO 3. Die meist verwendeten basischen Titriermittel sind NaOH, K 2 CO 3 oder Na 2 CO 3. Säure-Base-Titrationen lassen sich je nach Stärke der Säure und Base wie folgt klassifizieren. Starke Basen-Titrationen
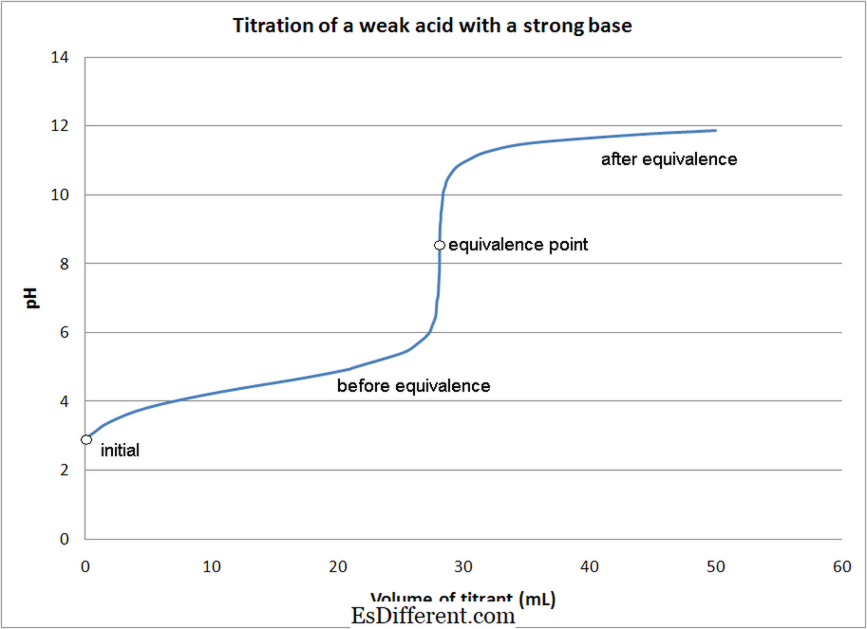
Schwache Säure - starke Basen-Titrationen- Schwache Säure - schwache Basen-Titrationen
- Bei der meisten Säure Basistitrationen werden Indikatoren verwendet, um den Endpunkt der Reaktion zu bestimmen. Je nach Art der Titration werden, wie oben erwähnt, verschiedene Indikatoren verwendet.
- Was ist eine Redox-Titration?
Eine Redox-Titration beinhaltet eine Redoxreaktion. Die Redoxreaktion hat zwei Reaktionen; eine Oxidationsreaktion und eine Reduktionsreaktion. Gleichzeitig finden sowohl Oxidations- als auch Reduktionsprozesse statt, bei denen man den Abschluß der Reaktion bestimmen kann. Dies ist auch als Endpunkt der Titration bekannt. Dies kann auf verschiedene Weise bestimmt werden; Indikatorelektroden, Redoxindikatoren (der Indikator erzeugt eine andere Farbe im Oxidations-Reduktions-Zustand) und Nicht-Redox-Indikatoren (Indikator erzeugt eine Farbe, wenn ein Überschuss an Titrant hinzugefügt wird).
Art der Reaktion:
Säure-Base-Titration:

Bei einer Säure-Base-Titration wird eine Neutralisationsreaktion zwischen dem Analyten (der Lösung mit unbekannter Konzentration) und dem sauren oder basischen Titrant durchgeführt.
Redox-Titration:
Eine Redox-Reaktion beinhaltet eine Oxidations- und Reduktionsreaktion zwischen dem Analyten und dem Titrant. Es gibt keine solche Regel, dass die Komponente oxidiert und welche reduziert wird. Entweder der Analyt oder der Titrant oxidiert, und die verbleibende Komponente verringert sich entsprechend. Bestimmung des Endpunktes:
Säure-Base-Titration: Zur Bestimmung des Endpunktes einer Säure-Base-Titration wird im Allgemeinen ein pH-Indikator, ein pH-Meter oder ein Konduktometer verwendet.
Redox-Titration:
Die am häufigsten verwendeten Methoden zur Bestimmung des Endpunktes einer Redoxreaktion sind die Verwendung eines Potentiometers oder eines Redoxindikators. Am häufigsten erzeugt jedoch entweder der Analyt oder der Titrant eine Farbe am Endpunkt. Damit sind in diesen Fällen keine zusätzlichen Indikatoren erforderlich. Beispiele:
Säure-Base-Titration: - diff Artikel Mitte vor Tabelle ->
Typ
Reaktion (Indikator)
Starke Säure - starke Basentitration

