Unterschied zwischen Kombinations- und Zerfallsreaktion | Kombinierte vs Zersetzungsreaktion
Schlüsselunterschied - Kombination vs. Abbaureaktion
Eine chemische Reaktion ist die Umwandlung einer oder mehrerer chemischer Verbindungen in eine oder mehrere chemische Verbindungen verschiedene Produkte, die die Identität einer chemischen Verbindung verändern. Das Ausgangsmaterial einer chemischen Reaktion wird Reaktant genannt, und die resultierende Verbindung wird Produkt genannt. Der Abbau von Verbindungen oder eine Kombination von Verbindungen und die Bildung neuer Verbindungen treten während eines chemischen Reaktionsprozesses auf, da die Bindungen zwischen Atomen der Verbindung gebrochen und auf andere Weise erzeugt werden. Chemische Reaktionen können in mehrere große Kategorien eingeteilt werden. Redox-Reaktionen oder Oxidations-Reduktions-Reaktionen sind unter ihnen sehr wichtig. Die Oxidations- und Reduktionsreaktionen werden Elektronentransferreaktionen genannt, da die Elektronen der Reaktanten von einer Verbindung zur anderen übertragen werden, um die Reaktion zu bewirken. Bei Redoxreaktionen treten gleichzeitig zwei parallele Reaktionen auf, die als Halbreaktionen bezeichnet werden. Diese Halbreaktionen zeigen die Übertragung von Elektronen. Durch Abwägen dieser Halbreaktionen kann man die Gesamtreaktion erahnen, die am Ende passiert ist. Kombinationsreaktionen und Zersetzungsreaktionen sind zwei Hauptarten von Redoxreaktionen. Der Hauptunterschied zwischen der Kombinations- und der Zersetzungsreaktion besteht darin, dass die Kombinationsreaktion eine Kombination von Reaktanten einschließt, um ein einzelnes Produkt zu ergeben, während die Zersetzungsreaktion 999 den Abbau einer einzelnen Verbindung in zwei oder mehr Produkte beinhaltet. INHALT 1. Übersicht und Tastendifferenz
2. Was ist eine Kombinationsreaktion3? Was ist eine Zerfallsreaktion
4? Seite an Seite Vergleich - Kombination vs. Zersetzungsreaktion
5. Zusammenfassung
Was ist eine Kombinationsreaktion?
Eine Kombinationsreaktion, die auch als
Synthesereaktion
bezeichnet wird, ist eine Reaktion, bei der die Reaktantenverbindungen kombiniert werden, um eine andere Verbindung als Produkt zu bilden. Mit anderen Worten, die Reaktion einfacher Moleküle führt zu einem komplexen Molekül. Einige oder alle Bindungen zwischen Atomen dieser bestimmten Verbindung werden abgebaut; Gleichzeitig werden sich Atome zur neuen Verbindung verbinden, die das Produkt ist. In Zersetzungsreaktionen wirkt derselbe Reaktant als Ausgangsmaterial für beide Halbreaktionen.Im Gegensatz zu Zersetzungsreaktionen haben die Halbreaktionen in Kombinationsreaktionen zunächst unterschiedliche Reaktanten. Kombinationsreaktion führt zu einem einzigen Produkt. Es folgt ein allgemeines Beispiel, das als Verbrennungsreaktionen angegeben werden kann.
Wenn zum Beispiel Aluminium (Al) in flüssigem Bromid (Br 2 ) platziert wird, tritt eine Kombinationsreaktion auf und erzeugt Aluminiumbromid (AlBr
3. Hier ist die Oxidationszahl in Al erhöht und in Br verringert. Daher handelt es sich um eine Redoxreaktion und um eine Kombinationsreaktion, da zwei Reaktanten umgesetzt wurden, um ein bestimmtes Produkt zu ergeben. Abbildung 01: Kombinationsreaktion
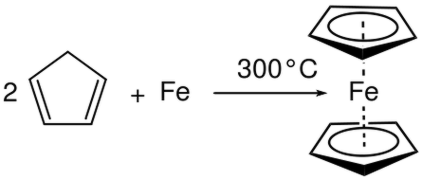
Bei der Elektrolyse von Wasser, wenn Gleichstrom durch Wasser geleitet wird, werden Wassermoleküle zu Sauerstoff- und Wasserstoffgasen zersetzt. Hier ist die Oxidationszahl im Sauerstoffatom erhöht und nimmt im Wasserstoffatom ab. Daher ist es eine Redoxreaktion und eine Zersetzungsreaktion aufgrund des Zerfalls von Wassermolekülen in Sauerstoff- und Wasserstoffgase.
Abbildung 02: Kombination vs. ZerfallWas ist der Unterschied zwischen Kombinations- und Zerfallsreaktion?
- diff Artikel Mitte vor Tabelle ->
Kombination vs. Zersetzungsreaktion

Zwei oder mehr Reaktionspartner sind an Kombinationsreaktionen beteiligt.
Eine einzelne Verbindung ist an einer Zersetzungsreaktion beteiligt.
Produkte
Kombinationsreaktion ergibt ein einziges Produkt. |
|
| Zersetzungsreaktionen führen zu mehreren Produkten. | Halbreaktionen |
| In Kombinationsreaktionen haben zwei Halbreaktionen zwei unterschiedliche Startmoleküle. | |
| In Zersetzungsreaktionen dient ein einzelnes Molekül als Ausgangsmaterial für beide Halbreaktionen. | Chemische Bindungen |
| Kombinationsreaktionen führen zur Bindung von Atomen, um das einzige Endprodukt zu erzeugen. | |
| In Zersetzungsreaktionen werden chemische Bindungen zu zwei oder mehr Endprodukten abgebaut. | Moleküle |
| Kombinationsreaktionen bewirken, dass einfache Moleküle reagieren und komplexe Moleküle produzieren. | |
| Zersetzungsreaktionen bewirken, dass komplexe Moleküle in einfache Moleküle zerfallen. | Zusammenfassung - Kombinierte vs Zersetzungsreaktion |
| Redoxreaktionen sind ein wesentlicher Teil der Welt um uns herum, da die meisten chemischen Reaktionen Redoxreaktionen sind. Kombinationsreaktionen und Zersetzungsreaktionen sind einfache Reaktionen, die einander entgegengesetzt sind. Der Hauptunterschied zwischen der Kombinations- und der Zersetzungsreaktion ist, dass die Kombinationsreaktion die Kombination von zwei oder mehr Reaktionsmolekülen einschließt, um ein einziges Endprodukt zu ergeben, während die Zersetzungsreaktion den Abbau eines einzelnen Moleküls in zwei oder mehr Produkte beinhaltet. | |
| Referenzen: | 1. Chang, R., 2010. Chemie. 10. Ausg. New York: McGraw-Hill. |
2. Redox. (2009, 30. Juli). Abgerufen 29. Mai 2017, von // weakinteractions. Wordpress. com / Primer / Redox /
3. Reaktionen. (n. d.). Abgerufen 29. Mai 2017, von // www. ric. edu / faculty / ptiskus / reactions /
Bild mit freundlicher Genehmigung:
1. "Miller Ferrocen Synthese" Von Bert. Kilanowski - Eigene Arbeit (CC0) via Commons Wikimedia
2. "Chemische Reaktionen" Von Daniele Pugliesi - Eigene Arbeit (CC BY-SA 3. 0) via Commons Wikimedia [Freigestellt]




