Unterschied zwischen Hydrolyse und Kondensation
Hydrolyse vs. Kondensation
Kondensation und Hydrolyse sind zwei Arten chemischer Reaktionen, die an der Bindungsbildung und dem Bindungsbruch beteiligt sind. Die Kondensation ist das Gegenteil der Hydrolyse. Diese zwei Arten von Reaktionen werden üblicherweise in biologischen Systemen gefunden, und wir verwenden diese Reaktionen auch, um viele kommerziell wichtige Produkte zu erhalten.
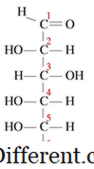
KondensationKondensationsreaktionen sind eine Art chemischer Reaktion, bei der sich kleine Moleküle zu einem großen Einzelmolekül zusammenschließen. Die Reaktion findet innerhalb von zwei funktionellen Gruppen in den Molekülen statt. Ein anderes charakteristisches Merkmal einer Kondensationsreaktion ist, dass während der Reaktion ein kleines Molekül verloren geht. Dieses Molekül kann Wasser, Chlorwasserstoff, Essigsäure usw. sein. Wenn das verlorene Molekül Wasser ist, sind diese Arten von Kondensationsreaktionen als Dehydratisierungsreaktionen bekannt. Da die Reaktantmoleküle kleiner sind und das Produktmolekül sehr groß ist, ist die Dichte der Produkte immer höher als die Reaktionen in Kondensationsreaktionen. Kondensationsreaktionen finden auf verschiedene Weise statt. Zum Beispiel können wir diese in zwei Arten als intermolekulare Kondensationsreaktionen und intramolekulare Kondensationsreaktionen unterteilen. Wenn sich die zwei funktionellen Gruppen im selben Molekül befinden, werden sie als intramolekulare Kondensationen bezeichnet. Zum Beispiel hat Glucose eine lineare Struktur wie folgt.
Dies ist eine Reaktion, bei der eine chemische Bindung mit einem Wassermolekül gebrochen wird. Während dieser Reaktion spaltet sich ein Wassermolekül in ein Proton und ein Hydroxid-Ion auf. Und dann werden diese zwei Ionen zu den beiden Teilen des Moleküls hinzugefügt, wo die Bindung gebrochen ist. Zum Beispiel folgt ein Ester. Die Esterbindung liegt zwischen -CO und -O.
Bei der Hydrolyse addiert sich das Proton aus dem Wasser zu der -O-Seite, und das Hydroxidion addiert sich zu der -CO-Seite. Als Folge der Hydrolyse bilden sich daher ein Alkohol und eine Carbonsäure, die bei der Bildung des Esters die Reaktanten sind.

Was ist der Unterschied zwischen Hydrolyse und Kondensation?




