Unterschied zwischen Mismatch Repair und Nucleotide Excision Repair | Mismatch Repair vs Nucleotide Excision Repair
Hauptunterschied - Fehlanpassung gegen Nukleotidexzisionsreparatur
Zehner und Tausende von DNA-Schäden treten in der Zelle pro Tag auf. Es induziert Veränderungen der Zellprozesse wie Replikation, Transkription sowie die Lebensfähigkeit der Zelle. In manchen Fällen können durch diese DNA-Schäden verursachte Mutationen zu schädlichen Krankheiten wie Krebs und altersassoziierten Syndromen führen (z. B. Progeria). Ungeachtet dieser Schäden initiiert die Zelle einen hoch organisierten Kaskadenreparaturmechanismus, der DNA-Schadensantwort genannt wird. Mehrere DNA-Reparatursysteme wurden im zellulären System identifiziert; Diese werden als Basenexzisionsreparatur (BER), Fehlpaarungsreparatur (MMR), Nukleotidexzisionsreparatur (NER), Doppelstrangbruchreparatur, bekannt. Die Nukleotidexzisionsreparatur ist ein sehr vielseitiges System, das DNA-Läsionen mit steriler Distortion erkennt und entfernt. Auf der anderen Seite ersetzt die Fehlpaarungsreparatur während der Replikation falsch eingebaute Basen. Der Hauptunterschied zwischen Fehlpaarungsreparatur und Nukleotidexzisionsreparatur besteht darin, dass Nukleotidexzisionsreparatur (NER) verwendet wird, um durch UV-Bestrahlung gebildete Pyrimidin-Dimere und sperrige Helix-Läsionen, die durch chemische Addukte verursacht werden, zu entfernen, während Fehlpaarungsreparatursystem eine wichtige Rolle bei der Korrektur von Fehlzerrungen spielt Basen, die während der Nachreplikation den Replikationsenzymen (DNA-Polymerase 1) entgangen sind. Zusätzlich zu fehlgepaarten Basen können MMR-Systemproteine auch die Insertions / Deletions-Schleifen (IDL) reparieren, die Ergebnisse der Polymerase-Slippage während der Replikation von repetitiven DNA-Sequenzen sind.
INHALT
1. Übersicht und Tastendifferenz
2. Was ist Mismatch-Reparatur
3. Was ist Nucleotide Excision Repair
4. Seite an Seite Vergleich - Fehlanpassung gegen Nukleotidexzisionsreparatur
5. Zusammenfassung
Was ist Nucleotide Excision Repair?
Das hervorstechendste Merkmal der Nukleotid-Exzisionsreparatur ist, dass es die durch signifikante Verzerrungen in der DNA-Doppelhelix verursachten modifizierten Nukleotidschäden repariert. Es wird in fast allen Organismen beobachtet, die auf dem neuesten Stand sind. Uvr A, Uvr B, Uvr C (Excinucleasen) Uvr D (eine Helicase) sind die bekanntesten Enzyme, die an der NER beteiligt sind und die Reparatur von DNA im Modellorganismus Ecoli auslösen. Uvr-ABC-Multi-Untereinheiten-Enzymkomplex produziert die Uvr A, Uvr B, Uvr C-Polypeptide.Die Gene, die für die oben genannten Polypeptide kodiert werden, sind uvr A, uvr B, uvr C. Uvr A- und B-Enzyme erkennen kollektiv die durch die UV-Bestrahlung hervorgerufene schädigungsinduzierte Verzerrung der DNA-Doppelhelix wie Pyrimidindimmer. Uvr A ist ein ATPase-Enzym und dies ist eine autokatalytische Reaktion. Dann verlässt Uvr A die DNA, während der Uvr BC-Komplex (aktive Nuklease) die DNA auf beiden Seiten des durch ATP katalysierten Schadens spaltet. Ein anderes Protein, das Uvr D genannt wird, das durch das uvrD-Gen kodiert wird, ist ein Helicase II-Enzym, das die DNA abspaltet, die aus der Freisetzung eines einzelsträngigen geschädigten DNA-Segments resultiert. Dies hinterlässt eine Lücke in der DNA-Helix. Nachdem das beschädigte Segment herausgeschnitten wurde, verbleibt eine 12-13 Nucleotide lange Lücke im DNA-Strang. Dies wird durch das DNA-Polymerase-Enzym I aufgefüllt und der Nucleus wird durch die DNA-Ligase versiegelt. ATP wird in drei Schritten dieser Reaktion benötigt. Der NER-Mechanismus kann auch bei Säugetier-ähnlichen Menschen identifiziert werden. Beim Menschen ist der Hautzustand, genannt Xeroderma pigmentosum, auf die durch UV-Bestrahlung verursachten DNA-Dimere zurückzuführen. Die Gene XPA, XPB, XPC, XPD, XPE, XPF und XPG produzieren Proteine, um DNA-Schäden zu ersetzen. Die Proteine der Gene XPA, XPC, XPE, XPF und XPG haben die Nukleaseaktivität. Auf der anderen Seite zeigen die Proteine der XPB- und XPD-Gene die Helicaseaktivität, die zu Uvr D in E coli analog ist.

Abbildung 01: Nucleotide Excision Reparatur
Was ist Mismatch Repair?
Das Mismatch-Reparatursystem wird während der DNA-Synthese initiiert. Sogar mit der funktionellen € -Untereinheit erlaubt die DNA-Polymerase III den Einbau eines falschen Nukleotids für die Synthese alle 10 8 Basenpaare. Mismatch-Reparaturproteine erkennen dieses Nukleotid, entfernen es und ersetzen es durch das korrekte Nukleotid, das für den endgültigen Grad der Genauigkeit verantwortlich ist. Die DNA-Methylierung ist für MMR-Proteine von entscheidender Bedeutung, um den Stammstrang aus dem neu synthetisierten Strang zu erkennen. Die Methylierung von Adenin (A) -Nucleotiden in einem GATC-Motiv eines neu synthetisierten Strangs ist etwas verzögert. Andererseits ist das Stamm-Adenin-Nukleotid im GATC-Motiv bereits methyliert. MMR-Proteine erkennen den neu synthetisierten Strang durch diesen Unterschied vom Stammstrang und beginnen die Fehlpaarungsreparatur in einem neu synthetisierten Strang, bevor er methyliert wird. Die MMR-Proteine richten ihre Reparaturaktivität aus, um das falsche Nukleotid zu exzidieren, bevor der neu replizierte DNA-Strang methyliert wird. Die Enzyme Mut H, Mut L und Mut S, die von den Genen mut H, mut L, mut S kodiert werden, katalysieren diese Reaktionen in Ecoli. Das Mut S-Protein erkennt sieben von acht möglichen Fehlpaarungs-Basenpaaren mit Ausnahme von C: C und bindet an der Fehlpaarungsstelle in der Duplex-DNA. Mit gebundenen ATPs verbinden sich Mut L und Mut S später mit dem Komplex. Der Komplex transloziert einige tausend Basenpaare, bis er ein hemimethyliertes GATC-Motiv findet. Die ruhende Nucleaseaktivität des Mut H-Proteins wird aktiviert, sobald es ein hemimethyliertes GATC-Motiv findet. Es spaltet den unmethylierten DNA-Strang, wobei ein 5 '-Nickel am G-Nucleotid des unmethylierten GATC-Motivs verbleibt (neu synthetisierter DNA-Strang).Dann wird der gleiche Strang auf der anderen Seite der Fehlpaarung von Mut H eingekerbt. In den übrigen Schritten schneiden die kollektiven Aktionen von Uvr D ein Helicase-Protein, Mut U, SSB und Exonuclease I das falsche Nukleotid im einzelsträngigen DNA. Die bei der Exzision gebildete Lücke wird von der DNA-Polymerase III aufgefüllt und durch Ligase verschlossen. Ein ähnliches System kann bei Mäusen und Menschen identifiziert werden. Die Mutation von humanem hMLH1, hMSH1 und hMSH2 ist an erblichem Nonpolyposis-Dickdarmkrebs beteiligt, der die Zellteilung von Kolonzellen dereguliert.
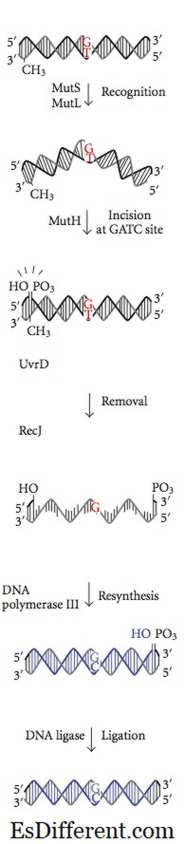
Abbildung 02: Mismatch Repair
Was ist der Unterschied zwischen Mismatch Repair und Nucleotide Excision Repair?
- diff Artikel Mitte vor Tabelle ->
Mismatch-Reparatur gegen Nucleotide Excision Repair |
|
| Mismatch-Reparatursystem tritt während der Post-Replikation auf. | Dies ist bei der Entfernung von Pyrimidin-Dimeren aufgrund von U. V-Bestrahlung und anderen DNA-Läsionen aufgrund eines chemischen Addukts beteiligt. |
| Enzyme | |
| Es wird von Mut S, Mut L, Mut H, Uvr D, SSB und Exonuklease I katalysiert. | Es wird von Uvr A, Uvr B, Uvr C, UvrD Enzymen katalysiert. |
| Methylierung | |
| Es ist entscheidend, die Reaktion zu initiieren. | Für die Initiierung der Reaktion ist keine DNA-Methylierung erforderlich. |
| Wirkung von Enzymen | |
| Mut H ist eine Endonuklease. | Uvr B und Uvr C sind Exonukleasen. |
| Anlass | |
| Dies geschieht speziell während der Replikation. | Dies geschieht bei der Exposition gegenüber U. V oder chemischen Mutagenen, nicht während der Replikation |
| Erhaltung | |
| Es ist hoch konserviert | Es ist nicht sehr konserviert. |
| Gap Filling | |
| Es wird durch DNA-Polymerase III durchgeführt. | Es wird durch DNA-Polymerase I durchgeführt. |
Zusammenfassung - Fehlpaarungsreparatur gegen Nukleotidexzisionsreparatur
Fehlpaarungsreparatur (MMR) und Nucleotidexzisionsreparatur (NER) sind zwei Mechanismen, die in der Zelle stattfinden, DNA-Schäden und Verzerrungen, die durch verschiedene Agenten verursacht werden. Diese werden kollektiv als DNA-Reparaturmechanismen bezeichnet. Nukleotidexzisionsreparatur repariert die modifizierten Nukleotidschäden, typischerweise jene signifikanten Schäden der DNA-Doppelhelix, die aufgrund der Exposition gegenüber UV-Bestrahlung und chemischen Addukten auftreten. Mismatch-Reparaturproteine erkennen das falsche Nukleotid, schneiden es ab und ersetzen es durch korrektes Nukleotid. Dieser Prozess ist für den endgültigen Grad der Genauigkeit während der Replikation verantwortlich.
Referenz:
1. Cooper, Geoffrey M. "DNA-Reparatur. "Die Zelle: Ein molekularer Ansatz. 2. Auflage. U.S. National Library of Medicine, 01. Januar 1970. Web. 09. März 2017.
2. "Mechanismen und Funktionen der DNA-Mismatch-Reparatur. "Zellforschung. U.S.-Nationalbibliothek der Medizin, n. d. Web. 09. März 2017.
Bild mit freundlicher Genehmigung:
1. "Nucleotide Excision Repair-Journal. pbio. 0040203. g001 "von Jill O. Fuss, Priscilla K. Cooper - (CC BY 2. 5) über Commons Wikimedia
2. "DNA Mismatch Reparatur Ecoli" Von Kenji Fukui - (CC BY 4. 0) über Commons Wikimedia