Unterschied zwischen Carbonsäure und Ester
Carbonsäure gegen Ester
Carbonsäuren und Ester sind organische Moleküle mit der Gruppe -COO. Ein Sauerstoffatom ist mit einer Doppelbindung an Kohlenstoff gebunden und der andere Sauerstoff ist mit einer Einfachbindung verbunden. Da nur drei Atome an das Kohlenstoffatom gebunden sind, hat es eine trigonal-planare Geometrie. Ferner ist das Kohlenstoffatom sp 2 hybridisiert. Die Carboxylgruppe ist eine weit verbreitete funktionelle Gruppe in der Chemie und Biochemie. Diese Gruppe ist die Muttergesellschaft verwandter Verbindungen, die als Acylverbindungen bekannt sind. Acylverbindungen sind auch als Carbonsäurederivate bekannt. Ester ist ein Carbonsäurederivat wie das.
Carbonsäure
Carbonsäuren sind die organischen Verbindungen mit der funktionellen Gruppe -COOH. Diese Gruppe ist als Carboxylgruppe bekannt. Carbonsäure hat eine allgemeine Formel wie folgt.
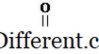
In der einfachsten Art von Carbonsäure ist die R-Gruppe gleich H. Diese Carbonsäure ist als Ameisensäure bekannt. Trotz Ameisensäure gibt es viele andere Arten von Carbonsäuren mit verschiedenen R-Gruppen. Die R-Gruppe kann eine gerade Kohlenstoffkette, eine verzweigte Kette, eine aromatische Gruppe usw. sein. Essigsäure, Hexansäure und Benzoesäure sind einige Beispiele für Carbonsäuren. In der IUPAC-Nomenklatur werden Carbonsäuren genannt, indem man den Endwert des e des Alkans, das der längsten Kette in der Säure entspricht, und durch Zugabe von -Säure fallen lässt. Dem Carboxyl-Kohlenstoff ist immer die Nummer 1 zugeordnet. Demnach ist der IUPAC-Name für Essigsäure Ethansäure. Anders als die IUPAC-Namen haben viele der Carbonsäuren gemeinsame Namen.
Carbonsäuren sind polare Moleküle. Wegen der -OH-Gruppe können sie starke Wasserstoffbrücken miteinander und mit Wasser bilden. Infolgedessen haben Carbonsäuren hohe Siedepunkte. Ferner lösen sich Carbonsäuren mit niedrigeren Molekulargewichten leicht in Wasser auf. Mit zunehmender Länge der Kohlenstoffkette nimmt jedoch die Löslichkeit ab. Carbonsäuren haben eine Acidität im Bereich von pKa 4-5. Da sie sauer sind, reagieren sie leicht mit Lösungen von NaOH und NaHCO 3, um lösliche Natriumsalze zu bilden. Carbonsäuren wie Essigsäure sind schwache Säuren, und sie befinden sich im Gleichgewicht mit ihrer konjugierten Base in wässrigen Medien. Wenn jedoch die Carbonsäuren elektronenziehende Gruppen wie Cl, F aufweisen, sind sie sauer als die unsubstituierte Säure.
Ester haben die allgemeine Formel RCOOR '. Ester werden durch die Reaktion zwischen einer Carbonsäure mit einem Alkohol hergestellt. Ester werden benannt, indem zuerst die Namen des alkoholischen Teils geschrieben werden. Dann wird der vom Säureteil abgeleitete Name mit der Endung -
ate oder - oate beschrieben.Zum Beispiel ist Ethylacetat der Name des folgenden Esters. Ester sind polare Verbindungen. Sie haben jedoch nicht die Fähigkeit, aufgrund des Mangels an Wasserstoff, der an Sauerstoff gebunden ist, starke Wasserstoffbrückenbindungen zueinander zu bilden. Im Ergebnis haben Ester niedrigere Siedepunkte im Vergleich zu Säuren oder Alkoholen mit ähnlichen Molekulargewichten. Oft haben Ester einen angenehmen Geruch, der die charakteristischen Gerüche von Früchten, Blumen usw. hervorbringt.

Was ist der Unterschied zwischen




